ステンレスの基礎知識
About stainless steel
ステンレスの一般的解釈
ステンレスとは「Stainless」のことで、「さびない」という意味です。実際には「さびにくい」とするのが正しい表現であり、ステンレス鋼は一般の鋼(鉄)と比較すると極めて優れた耐食性(材料が腐食作用に耐える性質)を有する材料です。クロム含有量を10.5%以上、炭素含有率を1.2%以下とし、耐食性を向上させた合金鋼をステンレス鋼といいます。
環境にもよりますが、ステンレスがより良い耐食性を持っているのは、その表面に作られているクロムの酸化被膜(一般に不動態皮膜と呼ばれる)の作用によるものです。
ステンレスの耐食性
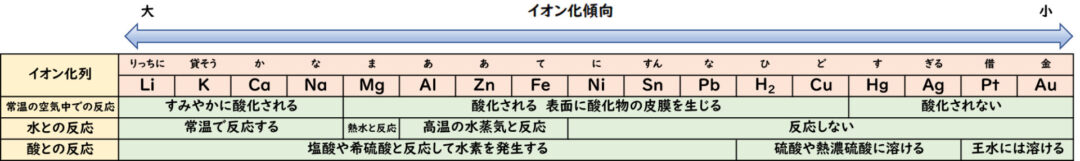
イオン化傾向
そもそも錆とは金属が空気中の酸素や水分と反応して酸化することによって発生するものです。金属のなかには、常温の大気や水と反応するものもあれば、酸としか反応しないものもあり、金属の種類によって化学反応の起こりやすさ(イオン化のしやすさ・イオン化傾向)は異なります。
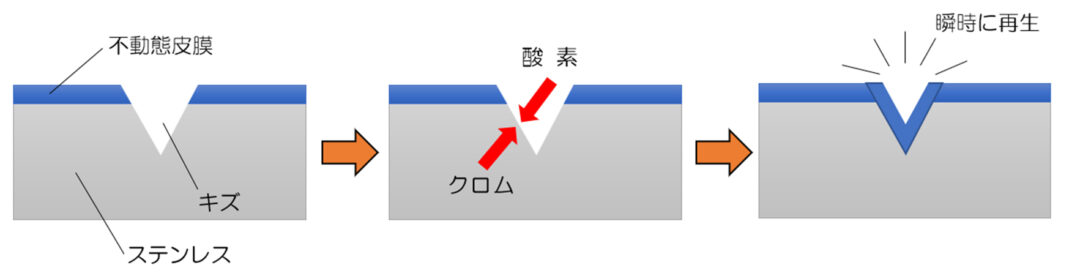
不動態皮膜
Au(金)やPt(白金)などの貴金属が、「化学反応を起こさない」ことで優れた耐食性を有するのに対して、ステンレスは大気中で酸化し、「不動態皮膜」という保護膜が表面に出来ることで耐食性を維持しています。この「不動態被膜」は傷がついてもすぐに再生されるという性質を持っています。
ステンレスの腐食性
ステンレス鋼は、大気中で酸化し「不動態皮膜」という保護膜が表面にできることで耐食性を維持しています。通常われわれが使用する中性の水環境において、ステンレス鋼はほとんど腐食しません。しかしステンレス鋼であっても腐食が発生する場合があります。
その一因として挙げられるのは塩化物イオン(Cl⁻)の存在です。使用環境中に塩化物イオンが存在すると、不動態皮膜が局部的に破壊され、この部分に穴があいたり(孔食)、応力が掛かっている状態では割れを生ずる(応力腐食割れ)引き金となることがあります。
・身近な塩化物イオンはどこにあるでしょうか?

塩化物イオンは私たちの身近な所にも存在しています。最初にイメージするのは、おそらく食卓にあるような食塩や、海水だと思います。それ以外にも塩素系の漂白剤や、融雪剤・凍結防止剤等様々なところに塩化物イオンは存在します。
海水に直接触れていなくても、潮風によって塩化物イオンが付着することもありますし、塩化物イオンが含まれている化学製品が付着することもあります。このように海以外のところでも、思いがけないところでステンレスの腐食が起こる場合もあります。
ステンレスの種類
「ステンレス」と一言でいっても、細かく分類すれば非常に多くの種類(鋼種)が存在します。「磁石にくっつくステンレスは安物だ」という言葉を耳にしたことはありますか?これは誤った考えで、磁石につく・つかないはステンレスの鋼種が異なるためであり、一概に「安物」であるとは言えません。
ステンレスは金属組織によって、マルテンサイト系・フェライト系・オーステナイト系析出硬化系・2相系(オーステナイト・フェライト)の大きく分けて5種類に分類されます。今回は一般的な3つのステンレスについて説明します。
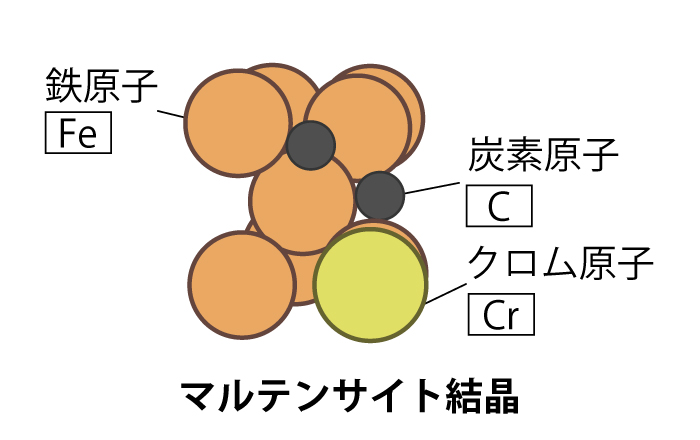
マルテンサイト系ステンレス
他の2種に比べ、炭素が多く含まれています。高温のオーステナイト組織から急冷(焼入れ)することによって、炭素が逃げられずに結晶格子が歪み、マルテンサイトという硬い金属組織になります。厳しい環境下で錆びやすく、ステンレス鋼の中で最も耐食性が劣ります。用途は、高強度、耐食性・耐熱性が必要なタービンブレード、ポンプ、シャフト、ノズルなどです。ナイフや包丁などの刃物としても使われます。
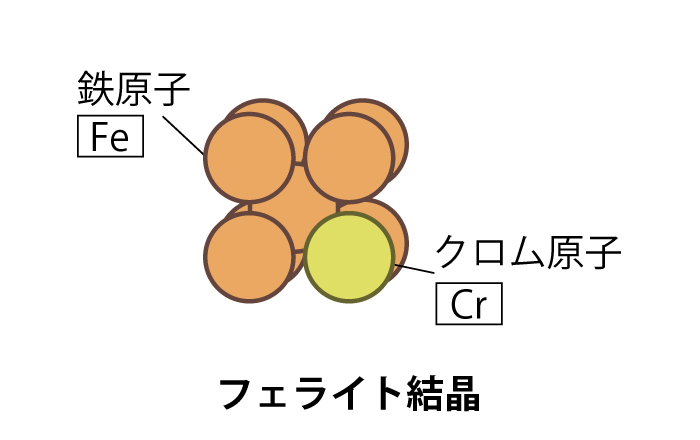
フェライト系ステンレス
常温でフェライトという金属組織になります。強度は高くありませんが、ニッケルを含まないためオーステナイト系と比較して安価な場合が多く、オーステナイト系に次ぐ耐食性をもちます。用途は、一般的な耐食性を要する厨房用品、建築内装、自動車部品、ガス・電気器具部品などです。強度がさほど高くないことや、比較的脆いことに注意が必要です。
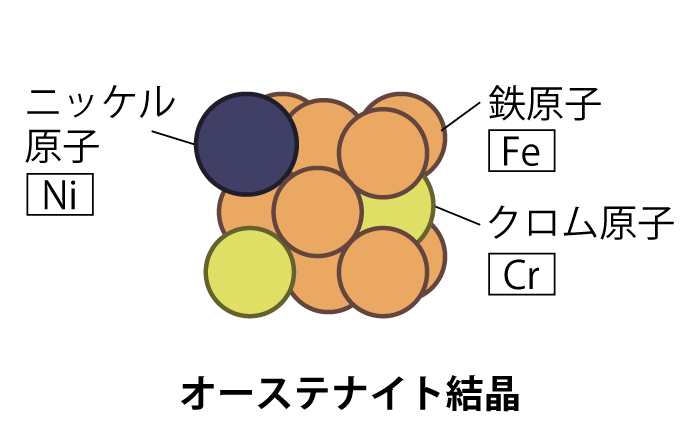
オーステナイト系ステンレス
ニッケルを含んでおり、常温でも高温でもオーステナイトという金属組織になります。耐食性に優れ、低温・高温での特性も優れます。延性・靭性に富み、深絞りや曲げ加工などの冷間加工性が良好で、溶接性にも優れます。また、冷間加工によって硬化するという性質もあります。(この時、磁石につくようになることがある。)
用途は、家庭用品、建築用品、自動車部品、化学プラントなど多種多様です。
以上のことから、オーステナイト系ステンレスは、チェーンや金具の製造に適した材料であるといえます。水本機械製作所で扱う製品はほとんどがオーステナイト系ステンレスです。
ステンレス鋼は使用する用途や目的によって、元素の種類や量が調整されています。それらを識別するためにJIS規格によって記号が定められています。下記表2は代表的な鋼種とその化学成分値をまとめたものです。
表1 ステンレスの種類と特徴
| 種類 | 鋼種の記号 | 化学成分 (wt%) | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| C | Si | Mn | P | S | Ni | Cr | Cu | Mo | ||
| マルテンサイト | SUS403 | 0.15以下 | 0.50以下 | 1.00以下 | 0.040以下 | 0.030以下 | - | 11.50~13.00 | - | - |
| SUS410 | 0.15以下 | 1.00以下 | 1.00以下 | 0.040以下 | 0.030以下 | - | 11.50~13.50 | - | - | |
| SUS420J2 | 0.26~0.40 | 1.00以下 | 1.00以下 | 0.040以下 | 0.030以下 | - | 12.00~14.00 | - | - | |
| フェライト | SUS430 | 0.12以下 | 0.75以下 | 1.00以下 | 0.040以下 | 0.030以下 | - | 16.00~18.00 | - | - |
| オーステナイト | SUS304 | 0.08以下 | 1.00以下 | 2.00以下 | 0.045以下 | 0.030以下 | 8.00~10.50 | 18.00~20.00 | - | - |
| SUS304J3 | 0.08以下 | 1.00以下 | 2.00以下 | 0.045以下 | 0.030以下 | 8.00~10.50 | 17.00~19.00 | 1.00~3.00 | - | |
| SUS316 | 0.08以下 | 1.00以下 | 2.00以下 | 0.045以下 | 0.030以下 | 10.00~14.00 | 16.00~18.00 | - | 2.00~3.00 | |
| SUS316L | 0.030以下 | 1.00以下 | 2.00以下 | 0.045以下 | 0.030以下 | 12.00~15.00 | 16.00~18.00 | - | 2.00~3.00 | |
| SUS310S | 0.08以下 | 1.50以下 | 2.00以下 | 0.045以下 | 0.030以下 | 19.00~22.00 | 24.00~26.00 | - | - | |
このように定まった成分規格に記号を与えることによって、多くの人が共通の認識で材料を扱うことが出来、それぞれの鋼種を性質の違いによって使い分けています。
ステンレスの熱処理
ステンレスに熱処理はつきものです。まずは主な熱処理の種類を以下に示します。
表1 熱処理の種類
| 熱処理の種類 | 内容 | 簡単なイメージ |
|---|---|---|
| 焼きなまし | 加工硬化による内部のひずみを取り除くことで、組織を軟化させて展延性を向上させる処理。 | 軟らかくして加工しやすくする。 |
| 焼入れ | オーステナイト組織の状態に加熱した後、水中又は油中で急冷し、マルテンサイト組織にする処理。 | 硬くする。 |
| 焼き戻し | マルテンサイト組織の状態から鋼を再加熱し、一定時間保持した後に冷却することで粘り強さを与える処理。 | 硬くしたものを少し軟らかくして、脆さを抑える。 |
| 固溶化熱処理 | 適温に加熱・保持し、材料の合金成分を固体の中に溶かし込み(固溶させる)、析出物を出さないように急冷する処理。 | 熱影響によって耐食性が低下した部分や、冷間加工による硬化を元通りにする。 |
ステンレスの種類つまり、マルテンサイト、フェライト、オーステナイトによって実施する熱処理は異なります。熱処理の方法や温度についても、JIS規格により鋼種ごとに定められています。弊社が主に扱っているオーステナイト系ステンレスは「固溶化熱処理のみ」となります。(表2参照)
表2 熱処理のJIS規格
| 鋼種 | 鋼種の記号 | 熱処理 | |||
|---|---|---|---|---|---|
| 焼なまし | 焼き入れ | 焼き戻し | 固溶化熱処理 | ||
| マルテンサイト | SUS403 | 800~900℃徐冷 又は約750℃急冷 |
950~1000℃ 油冷 |
700~750℃ 急冷 |
- |
| SUS410 | 800~900℃徐冷 又は約750℃急冷 |
950~1000℃ 油冷 |
700~750℃ 急冷 |
- | |
| SUS420J2 | 800~900℃徐冷 又は約750℃急冷 |
920~980℃ 油冷 |
600~750℃ 急冷 |
- | |
| フェライト | SUS430 | 780~850℃空冷 又は徐冷 |
- | - | - |
| オーステナイト | SUS304 | - | - | - | 1010~1150℃急冷 |
| SUS304J3 | - | - | - | 1010~1150℃急冷 | |
| SUS316 | - | - | - | 1010~1150℃急冷 | |
| SUS316L | - | - | - | 1010~1150℃急冷 | |
| SUS310S | - | - | - | 1030~1180℃急冷 | |
水本機械製作所で扱う製品はほとんどがオーステナイト系ステンレスなので、「固溶化熱処理」について少し詳しく説明します。
冷間加工によって発生するひずみによってSUS304は加工硬化します。また溶接を行うと、溶けた部分やその周辺の熱影響部は組織変化を起こします。これらの組織変化を起こした部分は、耐食性が低下している場合があります。これを均一なオーステナイトに戻し、耐食性を元通りにすることが固溶化熱処理の目的です。ただし同時に、冷間加工によって得られた硬さも失われることになります。
固溶化熱処理には、大気状態で行われる熱処理と真空や不活性ガス雰囲気中で行う熱処理があります。
大気熱処理
大気熱処理は、大気状態で加熱した炉の中に試料を入れ、昇温後取り出して水槽で冷却します。炉は昇温したまま連続使用出来るので、処理費用が真空や雰囲気熱処理と比較して安価ですが、表面に酸化物層が出来るので製品が黒くなってしまいます。その為、再度光沢を持たせるには酸洗や研磨などの後処理が必要となります。
雰囲気熱処置
雰囲気熱処理は、都度室温の炉内に試料を入れ密閉後にガス置換を行い、加熱・昇温した後に、窒素などの不活性ガスを流して冷却します。炉の大きさや冷却能力によって1回の処理量が制限される上に、多量の不活性ガスを使用し毎回炉内が室温になるので効率が悪く処理費用が高くなります。しかし高温処理にもかかわらず酸化はしないので光沢が維持されており、基本的には酸洗や研磨などの後処理が不要になります。